در بين تمامي کانسرهايي که ميشناسيم، کانسر ريه شايد بيشترين شيوع را نداشته باشد ولي بيشترين مورتاليتي را به خود اختصاص مي دهد.
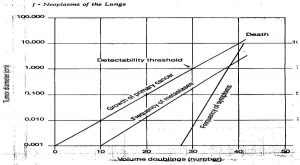
وقتي تومور ها شروع به رشد ميکنند، سايزشان که از يک حدي بيشتر شود شروع ميکنند به متاستاز دادن. در مورد کانسر ريه همانطور که در نمودار زير مي بينيد وقتي که تومور 30 تا doubling time doubling time( يعني مدت زماني که طول مي کشد تا حجم تومور 2 برابر يا در واقع قطر تومور 1.2 برابر شود. ما بيشتر قطر تومور را ميسنجيم چون در عکس ما دو بعد را مي بينيم.( را طي ميکند، قطري حدود 1 cm پيدا ميکند و بعد از 10 تا doubling time که قطرش 31 است، تومور شروع به متاستاز دادن ميکند. تا قبل از اينکه اندازه تومور به 0.8-1 cm برسد، هيچگونه عالئمي ندارد و تشخيص داده نميشود مگر اينکه در screening يافت شود در اين زمان تومور در حال متاستاز دادن است و وقتي توموري متاستاز بدهد يعني وارد 4 stage شده و در اين stage خيلي روي survival بيماران نميتوان حساب باز کرد )مگر در تومور هاي خاصي اما در تومور هاي ريه تومور به سرعت متاستاز ميدهد.( از 27 يا 28 امين doubling time تومور شروع ميکند به عالئم دادن و بين 30 تا 40 امين doubling time هم مراحل انتهايي بيماري است. يعني وقتي تومور را بر اساس عالئمي که دارد کشف مي کنيم که ديگه خيلي کار از کار گذشته !
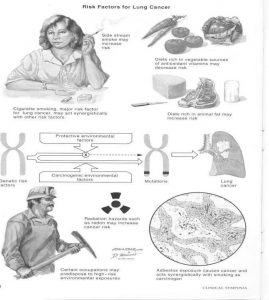 عوامل خطر :
عوامل خطر :تحقيقات نشان داده که بيشترين عاملي که با کانسر ريه در ارتباط است ، مصرف سيگار مي باشد. ريسک ابتال به کانسر ريه در افرادي که سيگار ميکشند، حدودا 20 برابر بيشتر از افرادي است که تا بحال سيگار نکشيده اند. خطر بروز کانسر ريه در ميان آنهايي که سيگار را ترک کرده اند در مقايسه با آنهايي که هنوز سيگار مي کشند کمتر است و اين خطر در آنهايي که قبال سيگاري بوده اند )بيشتر از 7 سال از ترک فرد گذشته( 9 برابر کساني است که هرگز سيگار نکشيده اند. کاهش خطر ابتال با مدت زمان ترک سيگار متناسب است. همسر فرد سيگاري بعنوان يک passive smoker نسبت به جمعيت عادي حدود 2 تا %30 ريسک افزايش يافته کانسر ريه دارد. )تاثير دود سيگار در محيط يا ETS يا دود دست دوم( اما آنهايي که همچنان فعاالنه سيگار مصرف ميکنند، %2000 در معرض ابتال مي باشند.
در جوامعي که مصرف سيگار در حال کنترل است و برنامه هايي براي پيشگيري و کاهش مصرف سيگار وجود دارد ميبينيم که موارد جديد ابتال به کانسر ريه هم در حال کاهش است. متاسفانه در جمعيت خانم ها مصرف سيگار رو به افزايش است.
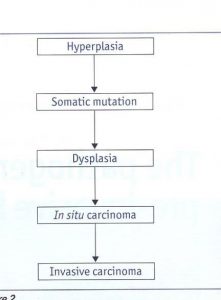
به ازا هر 15 نخ سيگار، يک جهش ژنتيکي در فرد رخ مي دهد و سير آن هم بدين صورت است که آسيبي به DNA وارد ميشود و موتاسيوني اتفاق مي افتد و ژن هاي سرکوبگر از بين ميروند و ژن هاي تهاجمي ايجاد ميشوند. اين موتاسيون هاي ژنتيکي در کسي که سيگار ميکشد هر روز اتفاق مي افتد و وقتي يک توالي از اين ها پشت سر هم قرار بگيرد، يک تغييراتي در بافت ايجاد ميکندکه اين تغييرات اينگونه است که هايپرپالزي توسط موتاسيون هاي سوماتيک به ديسپالزي و ديسپالزي هم توسط يک جهش جديد به کارسينوم درجا تبديل شده و موتاسيون جديد ديگري ميتواند آنرا به کارسينوم مهاجم تبديل کند.
يکي ديگر از ريسک فاکتورهاي کانسر ريه، رادياسيون گاز رادون است که هم در محيط هاي سر بسته خانه و هم در کارگراني که در معادني که گاز رادون متساعد ميشود کار ميکنند ديده ميشود. )مواجهه طوالني مدت با مقادير کم رادون در خانه در مقايسه با آنهايي که ETS محسوب ميشوند ميتواند خطر ابتال به کانسر برابر يا بيشتري داشته باشد.(
گفته ميشود که مواد غذايي که حاوي آنتي اکسيدان هستند، مثل ميوه جات و سبزيجات تازه، باعث ميشوند که ريسک کانسر ريه در افرادي که سيگار مصرف ميکنند کاهش پيدا کند ولي هنوز اثبات نشده که به اين ها توصيه کنيم که بتاکاروتن با دوز باال مصرف کنند که جلوي کانسر ريه را بگيرد.
از ساير کارسينوژن ها ميتوان به آرسنيک، آزبستوز، اتر، کروميوم، گاز Mustard، نيکل و هيدروکربن هاي پلي سيکليک اشاره کرد.
زمينه ژنتيکي هم در ايجاد کانسر ريه تاثير دارد. اقوام درجه يک فردي که کانسر ريه دارد، 2 تا 3 برابر خطر افزايش يافته ابتال به کنسر ريه دارند.
پاتولوژي:
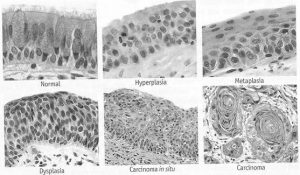
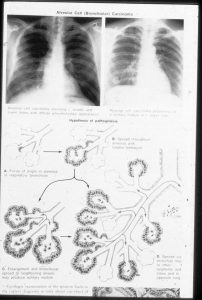
همانطور که در شکل باال ميبينيد در ابتدا سلولهاي استوانه اي کاذب مژکدار راه هاي هوايي روي غشاء پايه قرار گرفته اند. اين سلولها وقتي تحت تاثير محرک هاي محيطي مثل مصرف سيگار قرار ميگيرند، دچار هايپرپالزي و بعد دچار متاپالزي سنگفرشي ميشوند سپس بترتيب دچار ديسپالزي و کارسينوم درجا ميشوند و در نهايت از غشاء پايه عبور کرده و کارسينوم مهاجم ايجاد ميکند.
تومورهاي ريه را از نظر پاتولوژي به دو دسته تقسيم ميکنيم:
small cell lung cancer -1
non small cell lung cancer -2 )که شامل آدنوکارسينوما، کارسينوم سلول سنگفرشي و کارسينوم سلول بزرگ است(
درمان و مرحله بندي اين دو دسته تومور با هم متفاوت است و کانسر هاي non small cell بيماري هايي هستند که اگر در مراحل اوليه تشخيص داده شوند، ميتوان آنها را با جراحي درمان کرد ولي در کانسر small cell اصال درماني بصورت جراحي برايش وجود ندارد.
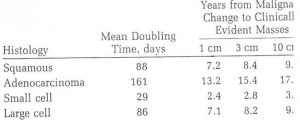
همانطور که در جدول باال مشاهده ميکنيد، در بين اين کانسرها، small cell نسبت به بقيه، doubling time کوتاه تري 29( روزه( دارد و آدنوکارسينوما بيشترين 161( DT روز( را دارد )يعني براي اينکه حجم تومور 2 برابر شود، 161 روز زمان الزم است.( پس small cell رشد سريع تري نسبت به بقيه دارد.
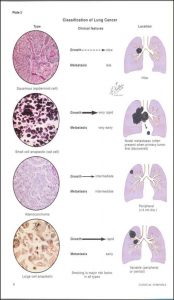
همانطور که در عکس مي بينيد، S.C.C و small cell تومورهاي سنترال هستند. تومور هايي که سنترال هستند، شانس اين را دارند که به راه هوايي راه پيدا کنند و باعث هموپتزي شوند. ولي تومورهايي مثل آدنوکارسينوما و large cell بيشتر پريفرال هستند؛ البته large cell ميتواند هم پريفرال و هم سنترال باشد )منظور از پريفرال و سنترال بودن، نسبت به راه هوايي اصلي است.(
شايعترين پاتولوژي تومورهاي ريه در آمريکاي شمالي آدنوکارسينوما است. )در کشور ما که نه آمار داريم و نه screening مناسب، ولي به نظر ميرسد که در ايران هم آدنوکارسينوما شايع تر باشد.(
در ميکروسکوپي S.C.C بين سلولهاي تغيير شکل يافته يک bridge و يک ارتباطي وجود دارد. pearl کراتيني هم ممکن است در بافت برش داده شده مشاهده شود. رشد اين تومور آهسته است 88( روز doubling time دارند(
Small cell lung cancer به سرعت متاستاز ميدهد )بدليل doubling time کوتاه 29 روزه سريع رشد کرده و متاستاز ميدهد.( و در مراحل اوليه بيماري متاستاز را داريم. يعني وقتي تومور را کشف ميکنيم همزمان با آن متاستازش را هم کشف ميکنيم )متاستاز به غدد لنفاوي ناحيه اي که قطعا داده!( ) داخل پرانتز : staging در کانسر ريه بر اساس TNM است.(
وقتي آدنوکارسينوما را در زير ميکروسکوپ نگاه ميکنيم ساختار غددي پيدا کرده. اين تومور يک رشد بينابيني دارد.
Large cell هم رشد سريعي دارد و هم زود متاستاز ميدهد. )البته بدخيم ترين و مورتال ترين در اينجا همانطور که گفتيم small cell است(
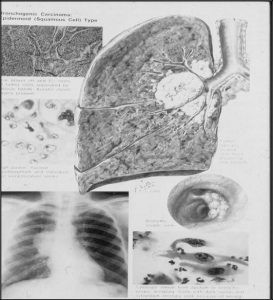
عکس زیر مربوط به تومور S.C.C مي باشد. که يک لوکيشن سنترال دارد و pearl کراتيني هم دارد. در chest X-ray هم ميبينيم که يک ضايعه مدور در ناف ريه سمت راست داريم )که مي بايست بطور طبيعي در اين محل دوشاخه شدن تراشه و عروق اينترلوبار را ميديديم(. در برونکوسکوپي هم يک برجستگي اينترابرونکيال ديده ميشود.
تصوير زیر يک کانسر large cell است که در واقع نه در پريفرال و نه در سنترال است. متاستاز هم داده. در زير ميکروسکوپ هسته هاي سلول بزرگ هستند.
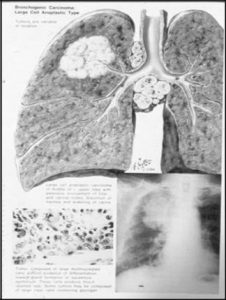
تصوير زیر مربوط به تومور small cell مي باشد. تومور وجود دارد و در پشتش يک پنوموني انسدادي ايجاد کرده و لنف نود ناحيه اي را هم درگير کرده. در کنار تومور يک ضايعه اقماري هم ميبينيم که در واقع يک سلول رشد کرده و بزرگ شده و هم به پارانشيم اطراف و هم به لنف نود هاي مجاور متاستاز داده. در پاتولوژي اين تومور وقتي ميخواهند سلول را به روي الم بکشند، هسته سلول چروکيده ميشود چون کرومانتين ظريف و شکننده اي دارند.
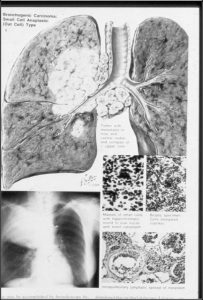
از روي ظاهر اين تومورها نميتوانيم نوع آن را تعيين کنيم و در واقع در ريه هرگاه ما شک به تومور داشته باشيم، بايد نمونه نسجي بگيريم.
در تصوير زير چند نوع از نمونه هاي تومور برونکيال را ميبينيم که ميتواند بصورت اندومورال )داخل ديواره( باشد و يا اندولومينال باشد و يا هم بصورت اکسترا لومينال و هم اينترالومينال رشد کرده باشد. )بسته به اينکه چه زماني آنرا کشف ميکنيم ميتواند گسترش هاي متفاوتي داشته باشد.(
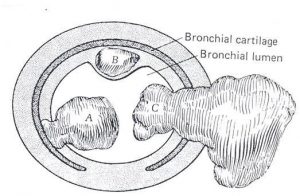
تومورهاي ريه معموال تمايل دارند که عالوه بر لنف نود هاي ناحيه اي به پلور، آدرنال، کبد، مغز و استخوان متاستاز بدهند.
عالئم:
مانند ساير تومورها، تومورهاي ريه هم يکسري عالئم فوکال يا regional دارند )يعني در همان منطقه اي که تومور وجود دارد عالئم را ايجاد ميکند.( يکسري عالئم هم بواسطه متاستاز به ساير ارگان ها مثل کبد و مغز و استخوان ايجاد ميشوند و يکسري هم تظاهرات پارانئوپالستيک هستند )يعني اثرات تومور را در جاهايي ميبينيم که تومور در آنجا وجود ندارد و بواسطه يکسري هورمون ها و موادي که توسط تومور ترشح ميشود، عالئمي را ايجاد ميکند. مثال تومور ADH ترشح کرده و روي کليه اثر ميگذارد و يا سيستم اتوايميون را تحت تاثير قرار ميدهد يا باعث دژنراسيون سلولهاي عصبي ميشود(
تظاهرات regional تومورها :
درگيري عصبي :)nerve entrapment( شايعترين موردي که داريم، درگيري عصب ريکارنت الرنژيال است که بيمار تغيير صدا يا خشونت صدا پيدا ميکند.داريم )تومورهايي اند که متاستاز ميدهند به آئورت و پولمونري و لنف نود هاي آنجا را درگير ميکنند باعث فشار به عصب ميشوند(.
ممکن است عصب فرنيک را که از داخل مدياستن عبور ميکند، درگير کند و باعث فلج ديافراگم و درنتيجه تنگي نفس شود )البته فلج يکطرفه ديافراگم باعث تنگي نفس در حال استراحت نميشود و فقط به هنگام فعاليت اتفاق مي افتد.(
در تصوير زير مشاهده ميکنيد که دست بيمار درد ميکند، افتادگي پلک )پتوز(، ميوز يا تنگي مردمک دارد و صورت بيمار)يک نيمه( تعريق نميکند؛ که بواسطه توموري است که در قله ريه وجود داشته )پان کوست تومور يا تومور شيار فوقاني( ، گسترش پيدا کرده و شبکه براکيال که عصب رساني دست را برعهده دارد درگير کرده و دست بيمار درد ميکند و الغر شده )سندرم پان کوست( و وقتي شبکه سمپاتيک به موازات نخاع را درگير کند، عالئم سيستم سمپاتيک )سندرم هورنر( که شامل پتوز و ميوز و عرق نکردن صورت است را هم نشان ميدهد.
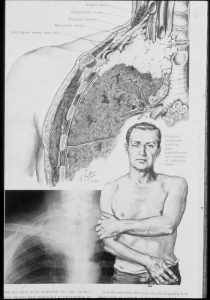
)هاريسون: سندرم پان کوست يا تومور شيار فوقاني ناشي از گسترش موضعي توموري است که در قله ريه رشد ميکند و با درگيري عصب هشتم گردني و اول و دوم سينه اي و درد شانه اي همراه است که از خصوصيات آن تيرکشيدن در مسير توزيع عصب اولنار در بازوست و اغلب با تخريب راديولوژيک دنده هاي اول و دوم همراه است. سندرم هورنر و سندرم پان کوست اغلب به همراه يکديگر وجود دارند.(
درگيري عروق :)vascular obstruction(
اگر توموري در داخل مدياستن رشد کند بيشتر ميتواند روي وريد )به نسبت شريان( اثر بگذارد چرا که تومور ميخواهد رشد و شريان ها جدار محکمي دارند ولي وريدها جدار داراي قابليت انعطافي دارند. بنابراين بر روي وريد فشار وارد کرده و سندرم SVC را ايجاد ميکند. )تصوير پايين( در سندرم SVC تخليه وريد SVC دچار مشکل شده و قدام قفسه سينه فرد قرمز است، صورت ورم کرده و پف آلودي دارد و وقتي بيمار دستهايش را باال مي آورد )که تخليه وريدي عروق سر و گردن را بيشتر دچار مشکل ميکند( صورت بيمار متورم و قرمز ميشود. اين حالت بيشتر در small cell lung cancer ديده ميشود.
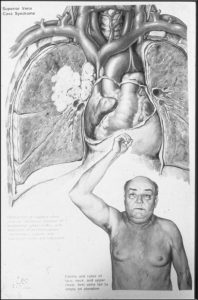
تومور ميتواند داخل شريان پولمونري رشد پيدا کند و آمبولي ريوي را تقليد کند.
ميتواند بر روي دريچه هاي قلب فشار وارد کند و تظاهرات تنگي دريچه پولمونري را ايجاد کند.
ميتواند به پريکارد انتشار پيدا کند و پريکارديال افيوژن و تامپوناد بدهد.
درگيري پلور :)pleural involvement(
در اينجا منظور ما پلورال افيوژن malignant است. )ما در زمينه بدخيمي ها دو نوع پلورال افيوژن داريم. يک حالت malignant داريم يعني داخل فضاي پلور سلولهاي بدخيم وجود دارد و متاستاز به داخل فضاي پلور هم اتفاق افتاده و يک حالت paramalignant داريم يعني پلورال افيوژني داريم که داخل آن سلولهاي بدخيم نداريم.( در کنار %9 تومورهاي ريه پلورال افيوژن هم داريم اما هميشه اين پلورال افيوژن خطرناک نيست و ميتواند بخاطر اين باشد که لنف نود هايي که مايع پلور را تخليه ميکنند درگير شده و تخليه فضاي پلور به درستي انجام نميشود.
درگيري مدياستن :)mediastinal extension(
تومور ميتواند به مري فشار وارد کرده و باعث اشکال در بلع و ديسفاژي شود.
وقتي تومور تخريب شد و وسط آن تخليه شد ميتواند بين مري و راه هوايي ارتباط و فيستول برقرار شود.
درگيري لنفاتيک :)lymphatic obstruction( در اينجا پلورال افيوژن paramalignant داريم.
در تصوير زير يک alveolar cell carcinoma را ميبينيم. يک زيرگروهي از آدنوکارسينوماهاي ريه هستند که به آنها کارسينوم سلول برونکوآلوئوالر )BAC( مي گويند. اينها يک رشد خزنده اي دارند يعني سلول از روي داربست بافت ريه رشد ميکند و اينگونه نيست که تومور خودش بخواهد يک توده اي را ايجاد کند.
بيمار ميتواند بصورت ترشحات بيش از حد از ريه اين سلولها را دفع کند و ترشحات ريوي زيادي داشته باشد )برونکوره(
همانطور که مشاهده ميکنيد اين تومور در عکس ريه هم خودش را بصورت يک توده نشان نميدهد و به شکل يک نماي شيشه مات )GGO( خودش را نشان ميدهد.
همانطور که گفتيم BAC و آدنوکارسينوم ريه شايعترين پاتولوژي کانسرهاي ريه در حال حاضر در سراسر جهان هستند که در خانم هاي نژاد شرقي که سيگاري نيستند، رو به افزايش است و خوشبختانه يک گيرنده اي )EGFR( بر سطح سلولها وجود دارد که ميتوانيم بر عليه آن آنتي بادي )مونوکلونال( بسازيم و بدين طريق رشد تومور را مهار کنيم. )در کل تومورهاي ريه اين پيشرفت در حال انجام است و آنتي بادي هاي مختلف در حال شناسايي اند که ميتوانند بروند و روي ژنوم تاثير بگذارند و رشد تومور را مهار کنند.(
در کانسر ريه هم مانند ساير کانسرها يکسري مارکرهاي توموري داريم )تصوير پايين( که يکسري از همين ها باعث عوارض پارانئوپالستيک تومور ميشود.
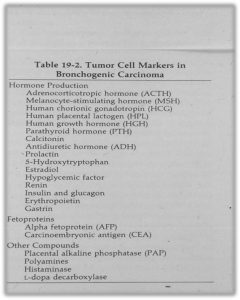
تظاهرات پارا نئوپلستيک کنسر ريه:
? تظاهرات اندوکرين:
-1هايپر کلسمي: تومور ريوي پارا تيروئيد هورمون (PTH) توليد ميکند و پارا تيروئيد هورمون کلسيم را از استخوان برداشته و سبب هايپر کلسمي ميشود . هيپرکلسمي شايعترين تظاهر تومور scc ريه است.
?-کوشينگ : تومور ريه ميتواند ACTH توليد کند و سبب ايجاد کوشينگ شود.
نکته: بيشترين تظاهرات پارا نئوپالستيک مربوط به small cell lung carcinoma است. اما هايپرکلسمي بيشتر مربوط به scc است.
?-ازدياد : ADH تومور مي تواند ADHتوليد کند.
?-ژنيکوماستي
:insulin_like activity -5 تومور IGF-1 ترشح ميکند. IGF-1 مشابه انسولين عمل ميکند .
: case بيمار توده اي در ريه خود دارد و با هيپوگاليسمي و افت سطح هشياري مراجعه ميکند . وقتي بررسي ميکنيم در ريه بيمار يک توده پيدا ميکنيم.
parathormone like effect :پاراتورمون توليد ميکند و هايپر کلسمي ايجاد ميکند. هايپر کلسمي موجب افزايش دفع آب از بدن، يبوست، لتالرژي و تشنج ايجاد مي شود.
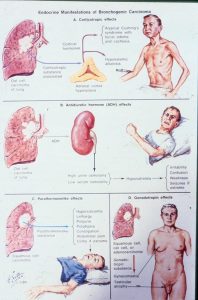
ADH effect : اين تومور باعث کاهش دفع آب از بدن ميشود و هايپو ناترمي ايجاد ميکند .تشنّج ، تغيير خلق و خو تا کما از عالئم هايپوناترمي است.
corticotropic effect تومور ACTH توليد ميکند و بر روي غده آدرنال تاثير مي گذرد و کورتيزول ترشح ميشود و عالئم کوشينگ پديد مي ايد.
افزايش بافت چربي گردن )گوژ پشت( ، صورت بر افروخته ، استرياي شکمي ، افزايش قند خون و هايپرتنشن از عالئم کوشينگ است.
gonadotropin effect : ميتواند عوارضي چون ژنيکوماستي و آتروفي بيضه ايجاد کند.
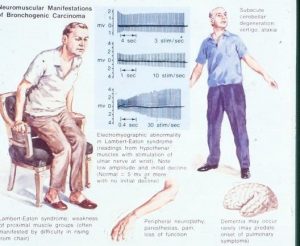
? تظاهرات نوروماسکوالر : اين تظاهرات بيشتر به علت فعاليت سيستم اتوايميون است . در واقع بر عليه سلولهاي تومورال آنتي بادي ترشح ميشود و به علت تشابه سلولهاي تومرال با ساختارهاي عصبي اينAb ها بر سلولهاي عصبي هم تاثير ميگذارند و اينگونه موجب تظاهرات عصبي ميشوند:
*انسفالوپاتي
*cerebellar degeneration
*نوروپاتي محيطي
*ميوپاتي کارسينوماتوز
*سندرم ايتون المبرت يا : stiffman syndrome اتو آنتي بادي بر عليه گيرنده استيل کولين اين بيماري را ايجاد ميکند . تظاهرات اين بيماري عکس بيماري مياستني گراويس است. در سندرم stiffman با انقباضات مکرر دامنه انقباض عضله زياد ميشود و بيمار مدام دچار انقباض عضله ميشود . اين هم از تظاهرات پارا نئوپالستيک smal cell lung cancerهست.
نکته : تظاهرات عصبي تومورهاي ريوي بسيار گسترده و وسيع است . غالبا اين تظاهرات مربوط به smal cell carcinomaاست.
? تظاهرات اسکلتال:
1 کالبينگ: کالبينگ بجز کنسر ريه در ILD ، برونشکتازي ، لنفوم هوچکين ،کرون هم ديده ميشود.
pulmonary hypertrophic osteoarthropathy – 2ياsubperiosteal new bone formation
:کالبينگ جزئي از اين بيماري هست اما معادل هايپر تروفيک استئوآرتروپاتي نيست. در اين بيماري در زير پريوسيت استخوانهاي دراز يک اليه ي جديد از استخوان تشکيل ميشود. رسوب کلسيم در زير پريوست اتفاق ميافتد و وقتي از استخوانهاي دراز بيمار عکس ميگيريم )در حالت نرمال( يک فضاي خالي وجود دارد ولي در هايپر تروفيک استئوارتروپاتي آن فضاي خالي از بين رفته است و کلسيم رسوب کرده است. در انتها استخوانهاي دراز اين اتفاق ميافتد .
? تظاهرات پوستي :
– اکانتوزيس نيگريکانس : تغيير رنگ قهوه اي پوست پشت گردن و چينهاي بدن را گويند . اکانتوزيس در ديابت تيپ ? هم ديده ميشود.
– اسکلرودرمي
? درگيريهاي عروقي:
– ترومبوفلبيت مهاجر يا سندرم ترسو : در سرطان پانکراس ديده ميشود و در سرطان ريه هم ديده ميشود.
– ترمبوزهاي شرياني
– اندوکارديت
? تظاهرات هماتولوژيک:
– آنمي – پلي سيتمي – ترومبوسيتوز
: Approach
اگر در عکس ريه تومور ديده شود بايد از آن نمونه نسجي تهيه شود و staging تومور بر اساس TNM )سايز تومور،لنف نود درگير ، متاستاز( مشخص شود.
TNM classificationهر چند سال بر اساس تغيراتي که در درمانها انجام ميشود ، عوض ميشود . stage Ia، Ib ، IIa مساوي هستند با جراحي staging. براي تعيين کردن نحوه درمان به کار ميرود. CT سايز و درگيري لنف نودها و متاستازهاي دور دست را نشان ميدهند.اگر ديديم بيمار سرطان ريه دارد بايد سر تا پاي بيمار CT شود.
• هدف در تومورهاي non small cell کشف زودرس تومور و جراحي است . جراحي تومور طول عمر بيمار را افزايش ميدهد.
اما اگر سايز تومور زياد شود و يا لنف نود ناحيه اي و لنف نود کنترالترل و يا لنف نود ساب کاريتل درگير ما از هدف )جراحي( دور ميشويم . وقتي متاستاز تومور به صورت لنف نود از مرکز اصلي دور ميشود ، ديگر نميشود آن ر ا با جراحي درمان کرد و بايد از شيمي درماني و راديو تراپي استفاده کنيم . بنابر اين TNM classification براي non small cell
cancersبه کار ميرود . از stage IIb شانس جراحي کم ميشود . در stage III به بعد هم که اصال جراحي توصيه نميشود و کموتراپي بايد انجام شود.
• براي small cell carcinoma ، TNMنداريم ، زيرا درمان small cell فقط راديوتراپي و شيمي درماني )کموراديوتراپي( است و جراحي فايده اي ندارد . small cell carcinoma در زمان تشخيص حتما حتما حتما متاستاز داده است و اگر جراحي کنيم مدتي بعد متاستازهايش در مغز ، استخوان ،آدرنال و… بروز ميکند.
solitary pulmonary nodule = SPN
گاهي اوقات يک توده منفرد در عکس ريه ديده ميشود . اطراف آن را پارنشيم ريه احاطه کرده است . : Case فردي براي استخدام شدن در کاري بايد عکس ريه بگيرد تا مشخص شود بيماري ريوي دارد يا نه. در عکس اين فرد يک SPN مشاهده ميشود که سايز آن کمتر از ? سانتي متر است و پارنشيم ريه اطراف آن را احاطه کرده است . متاستاز به لنف نود ناحيه اي ندارد . عالئمي هم در خارج از ريه ندارد.
تشخيصهاي افتراقي: spn به چند دسته ي خوش خيم ، بدخيم ، گرانولوم عفوني ، گرانولوم غيرعفوني و …. تقسيم مي شود.
بدخيم:
• : bronchogenic carcinoma سرطانهايي که در اين جلسه راجع به آن صحبت ميکنيم.
• لنفوم ريوي
• سارکوم ريوي
• ( plasmocytoma مالتيپل ميلوم نسجي(
• :solitary metastasis کولون ، کليه ، گردن ، سر ، breast، سلولهاي ژنيتال
• کارسينويد تومور
خوش خيم:
• هامارتوم : spn ميتواند يک نقص مادر زادي مثل هامارتوم باشد که وقتي آن را بيرون مياوريم در آن غضروف ، چربي و .… ديده شود.
• آدنوما
• ليپوم
گرانولوم عفوني :
• :TB مثال در گذشته TB گرفته و خوب شده ولي جاي آن به صورت يک ندول در ريه فرد باقي مانده است . )کمپلکس )marcus gannلنف نود ناحيه اي هم درگير است) tbوّليه(ا
• هيستو پالسما : در ايران نيست و در آمريکا شمالي وجود دارد.
• مايستوما )قارچ(
• آسکاريس
• اکينوکوکوس
• dog heart worm
گرانولوم غير عفوني: RA وگنر سارکوئيدوز Paraffinoma
:misscellaneous
-آبسهاي که تخليه نشده است.
BOOP-
– سيليکوز
– هامارتوما
:pseudo tumor- در CHF ، مايع در داخل فضاي پلور تجمع مييابد . گاهي مايع فقط در fissure تجمع مييابد و خود را به صورت يک mass در CXR نشان ميدهد . وقتي ديورتيک تجويز ميگردد آن massاز بين ميرود و در واقع يک تومور دروغين بوده است . نام ديگر آن phantom tumor است.
arteriovenous malformation-
– آميلوييدوما
– کيست برونکوژنيک
– فيبروز / اسکار
– انفارکت
همانطور که ديديم طيف وسيع از تشخيصهاي افتراقي براي SPN مطرح است. روشي وجود دارد که بتوان به کمک آن ندول را به انواع high risk و low risk تقسيم کرد و بر اساسHigh يا Low ريسک بودن اقدام الزم را انجام داد .در جدول زير چند آيتم )قطر تومور سنّ، بيمار ، سابقه مصرف سيگار ، وضعيت مصرف سيگار در حال حاضر و کاراکتر ندول ( مد نظر است . مصرف سيگار مهمترين ريسک فاکتور بدخيمي در ريه است. هر چهسنّ باالتر رود شانس ايجاد بدخيمي در ريه افزايش مييابد.
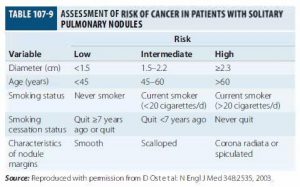
• اگر سايز تومور کمتر از ?.? سانتي متر باشد ، اگرسنّ بيمار کمتر از ?? باشد ، اگر کسي باشد که هرگز سيگار نکشيده است و يا در ? سال گذشته ترک کرده است و ديگر مصرف نکرده است ، اگر حاشيه ندول در عکس ريه صاف و گرد باشد ، اين بيمار low risk است و شانس بد خيم بودن SPN کمتر از %? است.
• اگر سايز تومور بيشتر از ?،? سانتي متر باشد ، سن بيمار بيشتر از ?? باشد ، smokerباشد و هرگز ترک نکرده باشد و اطراف تومور حالت شعاعي داشته باشد (corona radiata) اين SPN ، high risk تلقي ميشود و احتمال وجود بد خيمي بيشتر از %?? وجود دارد.
• اگر بيماري بيشتر از ?? سالسنّ داشته باشد (high) ولي بقيه خصوصيتش Low باشد باز هم high risk محسوب ميشود . پس اگر حد اقل يک ريسک فاکتور high داشته باشد مثال سايز آن بيشتر از ?.? سانتي متر باشد ، high risk محسوب ميشود. بر اساس اين روش SPN به سه نوع high ، intermediate،و low تقسيم ميشود و بر آسان آن تقسيم گيري انجام ميشود.
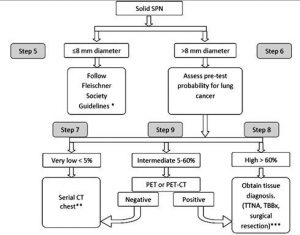
• اگر ندولي بيشتر از ? ميليمتر ديده شد و بر اساس معيارهاي گفته شده در دسته low risk قرار گرفت ) احتمال بد خيمي کمتر از %?( نياز به جراحي و درمان نيست و با Cerial CT بايد Follow شود . هر سه ماه يکبار بايد CT شود تا ببينيم ندول رشد ميکند يا نه . اگر تومور بدخيم باشد مثال ادنوکارسينوم باشد )??? روز)DT= در عرضه ? ماه بايد حد اقل يک DT را گذرانده باشد و قطر آن ?.? برابر شده باشد . اگر در Cerial CT افزايش سايز ندول مشاهده شد اين ندول بايد خارج شود.
• اگر ندول بزرگتر از ? ميليمتر بود و بر اساس معيارهاي گفته شده در دسته High risk قرار گرفت ) احتمال بد خيمي بيشتر از %?? ( بايد از آن نمونه نسجي ( (obtain tissue تهيه شود ، به کمک برونکوسکوپي ، نمونه برداري تحت گايد سونو يا CT و يا توسط جراح و از طريق . open biopsy
• اگر ندول بزرگتر از ?ميليمتر ديده شده بر اساس معيارهاي گفته شده در دسته intermediate risk قرار گرفت ) احتمال بد خيمي بين ? تا ?? % ( بايد از PET SCAN استفاده شود . در PET گلوکز نشان دار شده به بيمار تزريق ميشود . گلوکز نشان دار وقتي در بافت تجزيه ميشود اشعه متصاعد ميکند و اين اشعه اسکن ميشود . اگر PET مثبت شد بايد از ندول obtain tissue تهيه شود . اگرPET منفي شد ، cerial CTانجام ميشود.
• اگر قبل از ارزيابي ريسک ندول به ? خصوصيت بر خورديم نياز به بررسي بيشتر نيست و ندول خوش خيم است :
.1 عکسهاي ريه بيمار نشان ميدهد که از ? سال پيش سايز SPN تغييري نکرده است.
.2 وجود کلسيفيکاسيونهاي خوش خيم مثل pop corn calcification و bull’s eye و هامارتوم speckeld calcificationو eccentric classification دو کلسيفيکاسين بدخيم هستند.
در کلسيفيکاسيون( eccentric خارج از مرکز( ، توموري بوده که کلسيفيکاسيون داشته و حاال قسمتي از تومور شروع به رشد کرده و کلسيفيکاسيون را به حاشيه رانده است. در کلسيفيکاسيون speckeled ، کلسيم به صورت نقطه نقطه ديده ميشود.
سوال: چرا براي افراد low risk PET انجام نميشود ؟چون گرونه .? ? ميليون تومن هزينه دارد . در ايران کال ? دستگاه PET scan داريم . هيچ بيمه اي هم هزينههاي آن را قبول نميکند . )ايراني قهرمان ، ايراني پهلوان ( بعضي بيماران حاضر اند بميرند ولي ? ميليون تومان هزينه PET را ندهند.خرّم) آن کس که در اين محنت گاه خاطري را سبب تسکين است(
غربال گري سرطان ريه : خيلي خوبه روشي وجود داشته باشد که بتواند قبل از آن که سرطان ريه متاستاز داده باشد آن را کشف کند . CXR در آزمونهاي استخدامي براي آنکه ببينيم در ريه بيمار سال يا يک gross ، وجود دارد يا نه استفاده ميشود . ولي در واقع ارزش CXR براي پيدا کردن تومور مخفي هنوز مشخص نيست.
low dose helical CT scan روشي است که اخيرا در بيماراني که بيشتر از ?? pack year سيگار مصرف کرده اند و بين ??-?? سالسنّ دارند ، به منظور screening مورد استفاده قرار ميگيرد.
غربالگري در جمعيتي انجام ميشود که ريسک کنسر ريه را دارند و همچنين بتوان براي آن درمان انجام داد. مثال يک بيمار يک توموري دارد و طول عمر ? ساله دارد و ? سال ديگر کشف خواهد شد . حاال ما با يک روشي screening ميکنيم و تومور را ? سال بعد کشف ميکنيم و شخص سر ? سال بميرد. پس زماني غربالگري ميکنيم که براي آن درمان مناسب وجود داشته باشد . (cast / benefit)
اگر در جمعيت ??-?? سالي که?? pack year سيگار مصرف کرده اند، با CXR به دنبال تومور بگرديم ، از ? در هزار مرگ ناشي از کنسر ريه جلوگيري ميشود . در low dose CT ? در هزار کاهش مرگ و مير وجود دارد. در کشورهايي که کاهش يک در هزار مرگ اهميت دارد از CT low dose helical استفاده ميشود.
PETمثبت در کجا وجود دارد ؟ سرطان ريه ،TB، لنفوم
اگر سايز تومور خيلي کوچک باشد ، PET منفي کاذب ميدهد.